Celleforandringer i livmorhalsen
Celleforandringer kan være forstadier til kreft i livmorhalsen. Påvisning av celleforandringer gjør det mulig å gripe inn på et tidlig tidspunkt med tiltak som kan forhindre kreft.

Sist oppdatert:
5. sep. 2025
Innhold i artikkelen
Hva er celleforandringer i livmorhalsen?
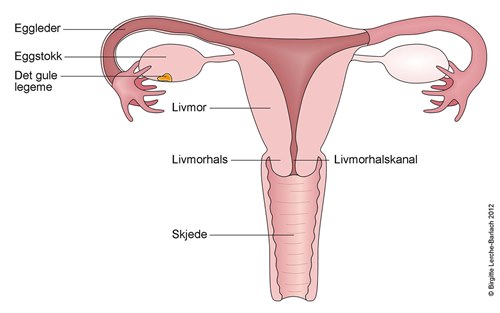
Celleforandringer kan være ufarlige forandringer som spontant forsvinner, eller det kan være forstadier til livmorhalskreft. Med forstadier menes forandringer som kan utvikle seg til kreft. I de fleste tilfeller vil celleforandringer ikke utvikles til kreft, men gå tilbake uten behandling —eller etter behandling når det er nødvendig.
I Norge får alle kvinner mellom 25 og 69 år tilbud om å delta i screening for livmorhalskreft. Undersøkelsen utføres vanligvis ved at fastlegen tar en prøve fra livmorhalsen.
Celleforandringer i livmorhalsen følger en trappemodell med stegvis endring fra lette forandringer til mer alvorlige, med livmorhalskreft i toppen av trappen. Celleforandringene kan snu underveis i trappen, der de lette celleforandringene snur oftere enn de moderate og grove. Dersom celleforandringene med tiden ikke normaliseres, eller ikke "snur i trappen", slik at det blir grovere celleforandringer, er behandling nødvendig. Det er dette som oppdages ved å ta regelmessige prøver i screeningprogrammet mot livmorhalskreft (Livmorhalsprogrammet).
Årsaker
I livmorhalsen er det i hovedsak HPV (humant papillomavirus) som forårsaker celleforandringene. HPV er en stor gruppe virus hvor rundt 40 typer smitter gjennom seksuell kontakt. Viruset kan medføre endringer i hud og slimhinner, hvor de vanligste endringene er kjønnsvorter og celleforandringer på livmorhalsen. HPV-infeksjon er den eneste kjente årsaken til livmorhalskreft.
Her kan du lese mer om infeksjon med humant papillomavirus.
Infeksjon med HPV er svært vanlig blant seksuelt aktive - mer enn sju av ti seksuelt aktive kvinner smittes i løpet av livet. Ny infeksjon er hyppigst blant unge voksne. Hos ni av ti kan man ikke se tegn til HPV etter to år.
Det er langvarig HPV-infeksjon som "driver frem" celleforandringene, og cellene normaliserer seg når infeksjonen ikke lenger kan påvises. For at celleforandringene skal føre til kreft må man for det første smittes med HPV, og så må infeksjonen vedvare lenge nok til å utvikle celleforandringer av mer alvorlig karakter. Det tar vanligvis rundt 15 år eller mer fra infeksjonstidspunktet til kreft oppstår.
Det er vist at HPV-infeksjon i livmorhalsen forekommer hyppigere hos kvinner som røyker, kvinner som har hatt mange seksualpartnere og kvinner med redusert immunforsvar.
Diagnostikk
Celleforandringer på livmorhalsen kan vanligvis ikke ses med det blotte øyet, og kvinnene det gjelder føler seg friske. Celleforandringer påvises ved mikroskopisk undersøkelse av en prøve tatt fra livmorhalsen. Livmorhalsprøven tas i forbindelse med gynekologisk undersøkelse, vanligvis etter et påminnelsesbrev fra screeningprogrammet mot livmorhalskreft —Livmorhalsprogrammet.
Livmorhalsprogrammet har over de siste årene vært i endring, både som følge av nye testmetoder og innføring av vaksine mot HPV. I løpet av 2023 ble tilbudet endret ved at alle kvinner mellom 25 og 69 år tilbys HPV-test hvert femte år som screeningmetode. Livmorhalsprøven undersøkes da på tilstedeværelsen av HPV. Dersom det ikke påvises HPV i prøven, anbefales vanligvis ny screeningprøve etter fem år. Selve prøvetakningen foregår som før.
I januar 2024 ble det vedtatt at det skal gjøres en såkalt utvidet genotyping dersom det påvises HPV-virus i livmorhalsprøven. Dette innebærer at videre utredning av kvinner med positiv HPV-test avhenger av hvilke HVP-virus typer som er påvist, kvinnens alder og cytologifunn. På denne måten blir oppfølgingen mer persontilpasset.
Grad av celleforandringer og HPV-type er blant faktorer som avgjør videre oppfølging. Videre oppfølging kan være at gynekologen utfører en kolposkopi. Dette innebærer at gynekologen studerer livmorhalsen ved hjelp av en spesialkikkert/mikroskop. I forbindelse med kolposkopien tar gynekologen også små vevsprøver, som sendes til laboratoriet for videre undersøkelse. Lett smerte kan oppleves når gynekologen tar vevsprøver. Det er mulig å be om lokalbedøvelse ved denne vevsprøvetakingen. Det kan også bli gjort en liten utskrapning av celler fra livmorhalsen. Det er vanlig å blø noe etter undersøkelsen.
Behandling
Dersom vevsprøvene tatt hos gynekologen viser alvorlige celleforandringer, anbefales behandling. Behandlingen går ut på å fjerne den helt ytterste biten av livmorhalsen, siden det er der celleforandringene er lokalisert. I noen tilfeller kan det være aktuelt å vente og se, med jevnlige kontroller, om forandringen forsvinner av seg selv.
Behandling består oftest av en såkalt "konisering". En kjegleformet bit ytterst på livmortappen fjernes med en liten elektrisk varmeslynge eller laser. En sjelden gang settes det noen sting for å stoppe blødning. Stingene løser seg opp av seg selv. Vevsbiten som fjernes, blir sendt til undersøkelse, og gynekologen mottar svar etter noen uker.
Konisering kan medføre svakhet i livmorhalsen ved graviditet, som igjen kan gi en lett økt risiko for senabort og for tidlig fødsel. Risikoen er størst der større deler av livmortappen er fjernet.
Les også Graviditet etter konisering.
Andre følgetilstander etter konisering kan være dannelse av et arrvev ytterst på livmortappen som kan gjøre det vanskelig å ta livmorhalsprøver etterpå, at det kan bli en stram ring i livmorhalsen som forsinker åpningsfasen under fødsel eller at det kan bli så arraktig trangt i livmorhalsåpningen at menstruasjonsblodet ikke kommer ut. Det siste er veldig sjeldent.
Etter slik behandling, anbefales fortsatt oppfølging med livmorhalsprøver, og i noen tilfeller kolposkopi. Informasjon om dette får man hos gynekologen eller fastlegen.
Forebygging av livmorhalskreft
Siden 1995 har alle kvinner i alderen 25 til 69 år fått tilbud om å ta regelmessig livmorhalsprøve. Både forekomsten og dødeligheten av livmorhalskreft er redusert, sammenlignet med perioden før innføring av screeningen.
Vaksinasjon mot HPV-infeksjon tilbys alle jenter og gutter i sjuende klasse i barnevaksinasjonsprogrammet. Vaksinen beskytter mot HPV-typene 16 og 18, som forårsaker sju av ti tilfeller av livmorhalskreft.
Kvinner som ønsker vaksine utenom barnevaksinasjonsprogrammet kan selv betale for HPV-vaksine og få denne satt på legekontoret.
Dette dokumentet er basert på det profesjonelle dokumentet Premaligne forandringer i cervix . Referanselisten for dette dokumentet vises nedenfor
- Helsedirektoratet (2016). Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av gynekologisk kreft [nettdokument]. Oslo: Helsedirektoratet; sist faglig oppdatert 05.05.2025. Siden besøkt 25.08.2025 www.helsedirektoratet.no
- Kreftregisteret. Kvalitetsmanual for Livmorhalsprogrammet. Oslo: Kreftregisteret; sist oppdatert 06.05.2025. Siden besøkt 25.08.2025 www.kreftregisteret.no
- Höhn AK, Brambs CE, Hiller GGR, et al. 2020 WHO Classification of Female Genital Tumors. Geburtshilfe Frauenheilkd. 2021 Oct;81(10):1145-1153. PMID: 34629493 PubMed
- Kreftregisteret. Årsrapport 2024. Screeningaktivitet og resultater fra Livmorhalsprogrammet. Oslo: Kreftregisteret, FHI; august 2025.
- Folkehelseinstituttet. Nøkkeltall for kreft. Livmorhalskreft. Oslo: FHI; sist endret 06.06.2025. Siden besøkt 25.08.2025 www.fhi.no
- Dillner J, Nygård M, Munk C et al. Decline of HPV infections in Scandinavian cervical screening populations after introduction of HPV vaccination programs. Vaccine. 2018 Jun 18;36(26):3820-3829. Epub 2018 May 31. PMID: 29778519 PubMed
- Nygård M, Engesæter B, Castle PE, Berland JM, et al. Randomized Implementation of a Primary Human Papillomavirus Testing-based Cervical Cancer Screening Protocol for Women 34 to 69 Years in Norway. Cancer Epidemiol Biomarkers Prev. 2022 Sep 2;31(9):1812-1822. PMID: 35793700 PubMed
- Gravitt PE. The known unknowns of HPV natural history. J Clin Invest. 2011 Dec;121(12):4593-9. Epub 2011 Dec 1. PMID: 22133884 PubMed
- Holl K, Nowakowski AM, Powell N, et al. Human papillomavirus prevalence and type-distribution in cervical glandular neoplasias: Results from a European multinational epidemiological study. Int J Cancer. 2015 Dec 15;137(12):2858-68. PMID: 26096203 PubMed
- Clifford GM, Smith JS, Plummer M, et al. Human papillomavirus types in invasive cervical cancer worldwide: a meta-analysis. Br J Cancer. 2003 Jan 13;88(1):63-73. PMID: 12556961 PubMed
- Folkehelseinstituttet. Flytskjema for HPV-screening. Oslo: FHI; sist endret 06.05.2025. Siden besøkt 25.08.2025 www.fhi.no
- Folkehelseinstituttet. Flytskjema for HPV-screening. Oslo: FHI; sist oppdatert 06.05.2025. Siden besøkt 27.08.2025 www.fhi.no
- Eide LM, Baasland I. Celleprøvetaking fra cervix - er det så vanskelig?. Gynekologen 2014; 27 (2): 32-4. www.legeforeningen.no
- Schiffman M, Castle PE, Jeronimo J, et al. Human papillomavirus and cervical cancer. Lancet 2007; 370 (9590): 890. PMID: 17826171 PubMed
- Depuydt CE, Criel AM, Benoy IH, et al. Changes in type-specific human papillomavirus load predict progression to cervical cancer. J Cell Mol Med. 2012 Dec;16(12):3096-104. PMID: 22978795 PubMed
- Tjalma WA, Fiander A, Reich O, Powell N, et al. HERACLES/SCALE Study Group. Differences in human papillomavirus type distribution in high-grade cervical intraepithelial neoplasia and invasive cervical cancer in Europe. Int J Cancer. 2013 Feb 15;132(4):854-67. PMID: 22752992 PubMed
- Burger EA, de Kok IMCM, Groene E, et al. Estimating the Natural History of Cervical Carcinogenesis Using Simulation Models: A CISNET Comparative Analysis. J Natl Cancer Inst. 2020 Sep 1;112(9):955-963. PMID: 31821501 PubMed
- Kaderli R, Schnüriger B, Brügger LE. The impact of smoking on HPV infection and the development of anogenital warts. Int J Colorectal Dis 2014. pmid:24935346 PubMed
- Jensen KE, Thomsen LT, Schmiedel S. Chlamydia trachomatis and risk of cervical intraepithelial neoplasia grade 3 or worse in women with persistent human papillomavirus infection: a cohort study. Sex Transm Infect 2014. PMID: 24728044 PubMed
- World Health Organization. Comprehensive cervical cancer control. A guide to essential practice. Second edition. Geneva: WHO; 2014. www.who.int
- Winer RL, Hughes JP, Feng Q, et al. Condom use and the risk of genital human papillomavirus infection in young women. N Engl J Med 2006; 354: 2645-54. PMID: 16790697 PubMed
- Trottier H, Mahmud S, Costa MC, et al. Human papillomavirus infections with multiple types and risk of cervical neoplasia. Cancer Epidemiol Biomarkers Prev 2006; 15: 1274-80. PMID: 16835323 PubMed
- Folkehelseinstituttet. HPV hjemmetest - for helsepersonell. Oslo: FHI; sist oppdatert 06.05.2025. Siden besøkt 27.08.2025 www.fhi.no
- Kreftregisteret. Hurtigtest for HPV kjøpt på nett – anbefales ikke av Livmorhals-programmet. Oslo: Kreftregisteret; sist oppdatert 14.01.2025. Siden besøkt 30.01.2025 www.kreftregisteret.no
- Koliopoulos G, Nyaga VN, Santesso N, et al. Cytology versus HPV testing for cervical cancer screening in the general population. Cochrane Database Syst Rev. 2017 Aug 10;8(8):CD008587. PMID: 28796882 PubMed
- Tropé A, Engesæter B, Nygård M, Andreassen T, Lönnberg S, Ursin G. Trygg implementering av HPV-testing i Livmorhalsprogrammet Safe implementation of HPV testing in the Norwegian Cervical Cancer Screening Programme. Tidsskr Nor Laegeforen. 2017 Sep 18;137(17). PMID: 28925234 PubMed
- Sørbye SW, Arbyn M, Fismen S, et al. HPV E6/E7 mRNA testing is more specific than cytology in post-colposcopy follow-up of women with negative cervical biopsy. PLoS One 2011; 6(10): e26022. pmid:21998748 PubMed
- Ronco G, Dillner J, Elfstrom KM, et al. Efficacy of HPV-based screening for prevention of invasive cervical cancer: follow-up of four European randomised controlled trials. Lancet 2013 Nov 1.Lancet. PubMed PMID: 24192252. PubMed
- Ogilvie GS, van Niekerk D, Krajden M, et al. Effect of Screening With Primary Cervical HPV-Testing vs Cytology Testing on High-grade Cervical Intraepithelial Neoplasia at 48 Months The HPV FOCAL Randomized Clinical Trial. JAMA 2018; 320: 43-52. pmid:29971397 PubMed
- Koliopoulos G, Nyaga VN, Santesso N et al. Cytology versus HPV- testing for cervical cancer screening in the general population. Cochrane Database Syst Rev 2017; 8: CD008587. PMID: 28796882 PubMed
- Gaustad J-V, Krontveit RI, Larsen MS. HPV-test i screeningprogrammet mot livmorhalskreft for aldersgruppen 25-33 år: systematisk oversikt. Oslo: Folkehelseinstituttet, 2022. www.fhi.no
- Arbyn M, Smith SB, Temin S et al. Detecting cervical precancer and reaching underscreened women by using HPV-testing on self samples: updated meta-analyses. BMJ 2018. pmid: 30518635 PubMed
- Polman NJ, Ebisch RMF, Heideman DAM et al. Performance of human papillomavirus testing on self-collected versus clinician-collected samples for the detection of cervical intraepithelial neoplasia of grade 2 or worse: a randomised, paired screen-positive, non-inferiority trial. Lancet Oncol 2019; 20: 229-38. pmid:30658933 PubMed
- Leinonen MK, Schee K, Jonassen CM et al. Safety and acceptability of human papillomavirus testing of self-collected specimens: A methodologic study of the impact of collection devices and HPV assays on sensitivity for cervical cancer and high-grade lesions. J Clin Virol 2018; 99: 22-30. pmid:29289814 PubMed
- Aasbø G, Tropè A, Nygård M et al. HPV self-sampling among long-term non-attenders to cervical cancer screening in Norway: a pragmatic randomised controlled trial. Br J Cancer. 2022 Nov;127(10):1816-1826. Epub 2022 Aug 23. PMID: 35995936 PubMed
- Skjeldestad FE, Hagen B, Hagmar B, Iversen O-E, Juvkam KH, Steen R, Thoresen S, Hareide B. Er cervixcytologisk undersøkelse av unge kvinner mer til skade enn til gagn?. Tidsskr Nor Lægeforen 2007; 127: 1782-5. PubMed
- Baasland I, Munk AC, Ernø LE et al. Cervixdysplasi i svangerskap (2020). Veileder i fødselshjelp. Oslo: Norsk gynekologisk forening; 2020. Siden besøkt 30.01.2025 metodebok.no
- Lycke KD, Kahlert J, Letersen LK, et al. Untreated cervical intraepithelial neoplasia grade 2 and subsequent risk of cervical cancer: population based cohort study. BMJ 2023; 383: e075925. pmid:38030154 PubMed
- Folkehelseinstituttet. HPV-vaksine (Humant papillomavirus) - håndbok for helsepersonell. Vaksinasjonshåndboka. Oslo: Folkhelseinstituttet, sist oppdatert 13.03.2025. Siden besøkt 25.08.2025 www.fhi.no
- Sand FL, Kjaer SK, Frederiksen K, Dehlendorff C. Risk of cervical intraepithelial neoplasia grade 2 or worse after conization in relation to HPV vaccination status. Int J Cancer. 2020 Aug 1;147(3):641-647. PMID: 31648368.
- Tainio K, Athanasiou A, Tikkinen KAO et al. Clinical course of untreated cervical intraepithelial neoplasia grade 2 under active surveillance: systematic review and meta-analysis. BMJ 2018; 360 :k499. PMID: 29487049 PubMed
- Koeneman MM, van Lint FHM, van Kuijk SMJ et al. A prediction model for spontaneous regression of cervical intraepithelial neoplasia grade 2, based on simple clinical parameters. Hum Pathol 2017; 59: 62-9. pmid:27697590 PubMed
- Bjørge T, Skare GB, Bjørge L, Tropé A, Lönnberg S. Adverse Pregnancy Outcomes After Treatment for Cervical Intraepithelial Neoplasia. Obstet Gynecol. 2016;128(6):1265-1273. PMID: 27824756 PubMed
- Kyrgiou M, Athanasiou A, Paraskevaidi M, et al. Adverse obstetric outcomes after local treatment for cervical preinvasive and early invasive disease according to cone depth: systematic review and meta-analysis. BMJ. 2016;354:i3633. Published 2016 Jul 28. PMID: 27469988 PubMed
- Kyrgiou M, Athanasiou A, Kalliala IEJ et al. Obstetric outcomes after conservative treatment for cervical intraepithelial lesions and early invasive disease. Cochrane Database of Systematic Reviews 2017, Issue 11. Art. No.: CD012847. DOI: 10.1002/14651858.CD012847. The Cochrane Library