Hypofysesykdommer
Sykdommer i hypofysen er ofte svulstsykdommer. Mange av disse svulstene produserer økte mengder av ett hormon, mens de kan medføre nedsatt produksjon av andre hormoner.

Sist oppdatert:
19. jan. 2021
Innhold i artikkelen
Hva er hypofysen?
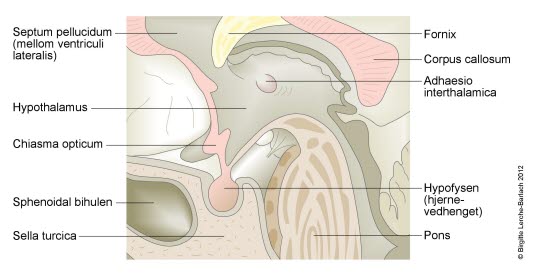
Hypofysen (hjernevedhenget) er en hormonproduserende kjertel som er en del av hjernen. Den kalles nedre hjernevedhenget fordi den ligger like under hjernen og er forbundet med hjernen med en kort nervestreng. Kjertelen er liten, den måler cirka en centimeter i diameter, og den veier cirka 0,5 gram. Kjertelen skiller ut flere typer hormoner som regulerer en lang rekke kroppsfunksjoner, deriblant en rekke livsviktige funksjoner.
Hypofysen og området ovenfor kjertelen, hypotalamus, fungerer tett sammen i reguleringen av kroppens hormoner. Forbindelsen mellom de to organene er kritisk for en normal hypofysefunksjon.
Hormonene som produseres, skilles ut i blodet, og bringes rundt til de områdene i kroppen hvor de har sin effekt. Hypofysen fungerer som en "termostat" for de livsviktige funksjonene i skjoldkjertelen og binyrene, den regulerer også funksjonen av våre indre kjønnsorganer (eggstokker og testikler) og er av avgjørende betydning for kroppens vekst og utvikling.
De hormonene som produseres i fremre del av hypofysen er: veksthormon (GH), tyreoideastimulerende hormon (TSH), adrenokortikotropt hormon (ACTH), luteiniserende hormon (LH), follikkelstimulerende hormon (FSH) og hormonet prolaktin (PRL). Bakre del av hypofysen skiller ut antidiuretisk hormon og oxytocin.

Hormonstyring
De enkelte hormonene produseres i bestemte deler av kjertelen.
Veksthormon (GH) dannes i og skilles ut fra hypofysen. Veksthormon er av avgjørende betydning for normal vekst og utvikling av de fleste av kroppens organer og funksjoner. Hovedeffekt er stimulering og utvikling av skjelett og muskulatur.
Tyreoideastimulerende hormon (TSH) har en stimulerende og regulerende effekt på skjoldkjertelen, som er den kjertelen som styrer kroppens stoffskifte.
Adrenokortikotropt hormon (ACTH) virker regulerende på funksjonen til kroppens to binyrer. Den mest betydningsfulle effekten er reguleringen av binyrenes utskillelse av kortisol. Kortisol er et hormon som også kalles kroppens stresshormon, og som er av avgjørende betydning for å sette kroppen i stand til å mestre alvorlige påkjenninger og overvinne sykdommer.
Follikelstimulerende hormon (FSH) og luteiniserende hormon (LH) kalles også gonadotropiner, det vil si at de har en stimulerende og regulerende effekt på kvinners eggstokker og menns testikler.
Prolaktin kalles også melkestimulerende hormon. Dette hormonet skilles ut i store mengder like etter svangerskap og fødsel, og prolaktin er en viktig forutsetning for melkeproduksjon og amming.
Hvordan oppstår sykdom?
Sykdommer kan oppstå på flere måter i hypofysen. Det hender at kjertelvevet i hypofysen vokser mer enn normalt. Dels skjer dette som en følge av økt behov for å stimulere andre kjertler i kroppen - for eksempel ved sviktende funksjon til testiklene (hypogonadisme), for å kunne øke produksjonen av det aktuelle hormonet. Økning i cellemassen på denne måten betegnes hyperplasi. Dels oppstår en kjertelsvulst (adenom) som kan være hormonelt aktiv. I slike tilfeller kan man se overproduksjon av hormoner fra den delen av kjertelen som vokser - noe som eksempelvis kan forårsake akromegali eller Cushings sykdom. Samtidig oppstår etterhvert svikt i produksjonen av andre hormoner. Unntaksvis forekommer også mer ordinære, hormonelt inaktive svulster i hypofysen (kraniofaryngeom og meningeom).
Hypofysen ligger i en liten lomme i skallebenet, og når kjertelen vokser, blir det etter hvert for trangt i denne lommen. På den måten kan en ellers uskyldig vekst av kjertelen føre til at kjertelen klemmes sammen, og etter hvert mister evnen til å produsere alle sine hormoner. Det oppstår hypopituitarisme, det vil si stimuleringen av de perifere kjertlene blir for liten, noe som igjen fører til nedsatt produksjon av hormoner i skjoldkjertelen, binyrene, etc.
Hjerneblødninger, svulster, strålebehandling mot hjernen eller bruk av cellegifter kan også føre til at hypofysen skades og hormonproduksjonen svikter.
Over- eller underproduksjon i hypofysen
Overproduksjon av veksthormon som starter før vekstsonene i skjelettet er lukket (barn), fører til unormal kroppsvekst og til det som kalles gigantisme. Etter at vekstsonene er lukket (voksne) vil økt mengde veksthormon føre til at skjelettet blir tyngre og grovere, og man kan se unormal vekst av ansiktsskjelett og hender og føtter (akromegali). Sviktende produksjon av veksthormon fører til forsinket vekst av skjelett og muskler eller muskelsvinn hos voksne.
Dersom det er overproduksjon av TSH, vil skjoldkjertelen overstimuleres og skille ut unormalt store mengder med stoffskiftehormon (tyroxin). Stoffskiftet blir da for høyt (hypertyreose). Ved sviktende TSH-produksjon vil stoffskiftet gradvis bli lavere (hypotyreose). Både for høyt stoffskifte og for lavt stoffskifte er sykdommer som uten behandling er livstruende. Men det finnes effektiv behandling for begge.
ACTH stimulerer og regulerer binyrenes produksjon av kortisol. Dersom det blir overproduksjon av ACTH, fører det til for store mengder kortisol i kroppen, en sykdom som kalles Cushing syndrom. Dette fører til en rekke endringer i kroppen med økt vekt, etter hvert benskjørhet og sviktende funksjon av en rekke livsviktige organer. Ved sviktende ACTH-produksjon i hypofysen får man kortisolmangel i kroppen (Addisons sykdom). Denne sykdommen medfører også alvorlige symptomer med generell svakhet i kroppen, redusert muskelstyrke, smerter, og svekket immunapparat. Behandling med kortisol (kortison tabletter) er livsnødvendig.
Addisons sykdom kan også starte med en akutt livstruende tilstand (Addison krise). Senere kan en slik krise også oppstå dersom tilførselen av kortisol blir for liten i forhold til behovet, for eksempel under en infekssjonssykom.
Sviktende produksjon av LH og/eller FSH fører til manglende utvikling og sviktende funksjon av kvinnens eggstokker og mannens testikler. Effektene blir menstruasjonsforstyrrelser, sviktende produksjon av kjønnshormoner og nedsatt fruktbarhet.
For høyt nivå av prolaktin utenom fødsel- og ammeperioder er den hyppigste hormonforstyrrelsen med utgangspunkt i hypofysen. Ofte skyldes det at den delen av hypofysen som produserer prolaktin, har vokst mer enn vanlig. For mye prolaktin fører til menstruasjonsforstyrrelser og svekket evne til å bli gravid hos kvinner, og til impotens hos menn.
Diagnostikk
Som beskrevet over kan sykdommer i hypofysen føre til over- eller underproduksjon av ett eller av flere av de hormonene som hypofysen normalt produserer. Dette kan gi mange forskjellige kroppslige utslag og forskjellige sykdomsbilder. Mange av sykdommene er alvorlige sykdommer som uten behandling er livstruende.
Pasientens beskrivelse av sine plager, og legens undersøkelse kan føre til mistanke om forstyrret hypofysefunksjon. Bekreftelse av diagnose krever analyse av blodprøver. Alle hormonene som produseres i hypofysen, kan analyseres i blod. Og forstyrret hormonproduksjon i skjoldkjertel, binyrer eller eggstokker/testikler kan også påvises i blodprøve. Når det er påvist hormonforstyrrelse, er det som regel nødvendig med ytterligere kartlegging med MR av hypofysen og eventuelt også de andre hormonproduserende organene for å kartlegge tilstanden.
Behandling
Hypofysesykdommer er hver for seg sjeldne, og behandlingen er komplisert. Hypofysesykdommer behandles derfor som regel ved sykehus eller av spesialister i hormonsykdommer (endokrinologer).
Behandlingen består av å tilføre de hormonene som kroppen ikke lenger produserer tilstrekkelig av (tyroksin, kortisol, testosteron, veksthormon), eller å bremse overproduksjon i hypofysen. Overproduksjon av prolaktin kan dempes med medisiner. Overproduksjon av veksthormon eller ACTH krever som regel operasjon for å fjerne den overaktive delen av kjertelen.
Dette dokumentet er basert på det profesjonelle dokumentet Hypofysesykdommer . Referanselisten for dette dokumentet vises nedenfor
- Chehade JM, Sultan S. Assessment of pituitary mass. BestPractice, last updated July 29, 2013.
- Lake MG, Krook LS, Gruz SV. Pituitary adenomas: an overview. Am Fam Physician 2013; 88: 319-27. American Family Physician
- Melmed S. Pituitary-tumor endocrinopathies. N Engl J Med 2020; 382:937-950. doi:10.1056/NEJMra1810772 DOI
- Lund-Johansen M, Aanderud S, Schreiner T, et al. Ikke-hormonproduserende hypofyseadenomer. Tidsskr Nor Lægeforen 2003; 123: 2253-6. PubMed
- Gittleman H, Ostrom QT, Farah PD, et al. Descriptive epidemiology of pituitary tumors in the United States, 2004-2009. J Neurosurg 2014;121:527-535. PubMed
- Iacovazzo D, De Marinis L. Treatment of hyperprolactinemia in post-menopausal women: pros. Endocrine. 2015 Feb;48(1):76-8. doi: 10.1007/s12020-014-0377-9 DOI
- Jørgensen AP, Bollerslev J. Hyperprolaktinemi. Nasjonal veileder i endokrinologi. Sist oppdatert 03.01.2020. www.endokrinologi.no
- Osa LE, Horjen J, Aanderud S, Lund-Johansen M. Operativ behandling av hormonproduserende hypofyseadenomer. Tidsskr Nor Lægeforen 2006; 126: 1330-2. PubMed
- Rogers A, Karavitaki N, Wass JA. Diagnosis and management of prolactinomas and non-functioning pituitary adenomas. BMJ. 2014;349:g5390. doi: 10.1136/bmj.g5390. DOI
- Svartberg J, Carlsen J, Cappelen J, Aanderud S, Lund-Johansen M, Schreiner T et al. Hyperprolaktinemi og prolaktinom - utredning og behandling Tidsskr Nor Lægeforen 2002; 122: 494 - 8.
- Higham CE, Johannsson G, Shalet SM. Hypopituitarism.Lancet. 2016 Nov 12;388(10058):2403-2415. doi: 10.1016/S0140-6736(16)30053-8. Epub 2016 Mar 31. PMID: 27041067. PubMed
- Eda M, Saeki N, Fujimoto N, Sunami K. Demonstration of optic pathway in large pituitary adenoma on heavily T2 weighted MR images. Br J Neurosurg 2002; 16: 21 - 9. PubMed
- Famini P, Maya MM, Melmed S. Pituitary magnetic resonance imaging for sellar and parasellar masses: ten-year experience in 2598 patients. J Clin Endocrinol Metab 2011;96:1633-1641. PubMed
- Chin BM, Orlandi RR, Wiggins RH 3rd. Evaluation of the sellar and parasellar regions. Magn Reson Imaging Clin N Am 2012;20:515-543. PubMed
- Jørgensen AP, Bollerslev J, Øystese KA, et al. Hypofyseadenom. Nasjonal veileder i endokrinologi, 26.02.2020. www.helsebiblioteket.no
- Gittoes NJL, Bates AS, Tse W, Bullivan B, Shephard MC, Clayton RN et al. Radiotherapy for pituitary tumours. Clin Endocrinol (Oxford)1998; 48: 331 - 7. PubMed
- Turner HE, Stratton IM, Byrne JV, Adams CBT, Wass JAH. Audit of selected patients with non-functioning piuitary adenomas treated without irradiation - a follow-up study. Clin Endocrinol (Oxford) 1999; 51: 281 - 4. PubMed
- Thoren M, Høybye C, Grenback E, Degerblad M, Rahn T, Hulting AL. The role of gamma knife radiosurgery in the management of pituitary adenomas. J Neurooncol 2001; 54: 197 - 203. PubMed
- Lillehei KO, Kirschmann DL, Kleinschmidt-Demasters BK, Ridgway EC. Reassessment of the role of radiation therapy in the treatment of endocrine inactive pituitary macroadenomas. Neurosurgery 1998; 43: 432 - 9. PubMed
- Suhardja A, Kovacs K, Rutka J. Genetic basis of pituitary adenoma invasiveness: a review. J Neurooncol 2001; 52: 195 - 204. PubMed
- Jonsson B, Nilsson B. The impact of pituitary adenoma on morbidity. Increased sick leave and disability retirement in a cross-sectional analysis of Swedish national data. Pharmacoeconomics 2000; 18: 73 - 81. PubMed
- Bates AS, Bullivant B, Sheppard MC, Stewart PM. Life expectancy following surgery for pituitary tumors. Clin Endocrinol 1999; 50: 315 - 9. PubMed
- Rosén T, Bengtsson B-Å. Premature mortality due to cardiovascular diseases in hypopituitarism. Lancet 1990; 336: 285 - 8. PubMed