Tykktarmskreft og endetarmskreft
Kreft i tykktarm eller endetarm, kolorektal kreft, er en av de vanligste kreftformene i Norge. Overlevelsen er svært god dersom sykdommen blir oppdaget på et tidlig tidspunkt.
Sist oppdatert:
9. apr. 2026
Innhold i artikkelen
Hva er kolorektal kreft?
Kolorektal kreft er en kreftsvulst i tykktarmen eller endetarmen. Kolon er det medisinske navnet på tykktarmen, hvor rektum (endetarmen) utgjør den siste delen. I de aller fleste tilfellene er svulsten utgått fra kjertelvev i tarmslimhinnen (adenokarsinom).
I Norge påvises rundt 3500 nye tilfeller av tykktarmskreft og vel 1400 nye tilfeller av rektumkreft hvert år. Tykktarmskreft er litt vanligere blant kvinner enn blant menn, mens det er motsatt for endetamrskreft.
Jo eldre man blir, jo større er sjansen for å utvikle kreft i tykktarmen. Antall tilfeller av tykktarmskreft blant personer under 50 år har imidlertid vært økende de siste årene. Man tror at årsaker til dette kan være knyttet til forekomsten av overvekt og fedme, kostholdsfaktorer, livsstil og endringer i bakteriesammensetningen i tarmen (mikrobiomet).
Årsaker
Hos de aller fleste har man ingen direkte forklaring på hvorfor sykdommen oppstod. Både genetiske og miljømessige faktorer spiller en rolle. Etterhvert har forskningen avdekket en rekke arvelige faktorer og mulige miljømessige og livsstilsmessige faktorer.
Miljø- og livsstilsfaktorer
Røykere har økt risiko for kolorektalkreft og andre kreftformer. Personer behandlet for kolorektalkreft som fortsetter å røyke etter behandling, har økt risiko for tilbakefall. Det er også funnet en økt risiko ved inntak av alkohol, risiko er sett å øke med økende inntak.
Overvekt og fedme samt høyt blodsukker er også sett å ha en sammenheng med økt risiko for kolorektalkreft. Det samme gjelder lav mengde fysisk aktivitet.
Når det gjelder kosthold er det gjort en lang rekke studier og funnet en rekke sammenhenger med faktorer i kosten. Mye av forskningen om kreft og kosthold er usikker kunnskap som først og fremst bygger på observasjoner av folkegrupper. I slike studier kan en finne sammenhenger, men ikke trekke sikre konklusjoner om direkte årsaksfaktorer. De fleste er imidlertid enige om at høyt inntak av rødt kjøtt og prosessert kjøtt øker risikoen for kreft i tykk- og endetarm. Kosthold med høyt innhold av fiber, frukt og grønnsaker er sett å redusere risikoen.
Arvelig tykktarmskreft
Forekomst av kreft hos søsken eller foreldre, og da spesielt tykktarmskreft, øker risikoen for at man selv kan utvikle kreft.
Det er funnet flere kjente genforandringer som øker risikoen for tykk- og endetarmskreft og man snakker da om arvelig tarmkreft. I noen familier ses opphopning av tykk- og endetarmskreft uten at man finner en kjent genfeil som årsak, dette kalles familiær økt risiko for tarmkreft. Familiær tarmkreft er hyppig og anslås å våre årsak i opptil to av ti tilfeller.
Arvelig (genetisk) tykk- og endetarmskreft med kjente genfeil omfatter blant andre Lynch syndrom, familiær adenomatøs polyppose (FAP) og MutYH-assosiert polyppose (MAP). Opptil tre prosent av alle med kolorektal kreft har en genetisk medvirkende årsak.
Lynch syndrom forekommer i ulike varianter, men felles er økt risiko for tykk- og endetarmskreft og andre kreftformer, blant annet livmorkreft. Risiko for tarmkreft i løpet av livet er anslått å være mellom 10 og 50 prosent ved Lynch syndrom.
FAP og MAP er såkalte polypposesyndromer. Det innebærer en økt tendens til å utvikle polypper og kolorektalkreft på grunn av en kjent genforandring i APC-genet eller MUTYH-genet. Mest alvorlig av disse er FAP der risiko for tarmkreft er tilnærmet 100 prosent innen 40 års alder blant de som ikke får oppfølging og behandling. Ved FAP anbefales regelmessige kontroller med endoskopi og de fleste opereres forebyggende ved å fjerne tykk- og endetarm.
Tarmsykdommer som Crohns sykdom og ulcerøs kolitt kan også gi noe økt risiko for å få kreft i tykktarmen, først og fremst ved alvorlig sykdom i mange år.
Symptomer
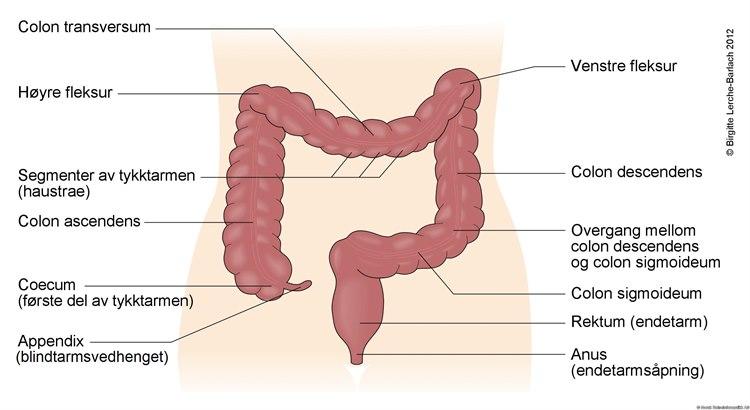 Tykktarmen
TykktarmenSvulstens plassering kan ha betydning for symptomer og funn ved tarmkreft. Ofte vokser svulsten langsomt, og den vil kunne presentere seg på ulike måter. Forenklet kan man skille mellom svulster som oppstår i høyre del av tykktarmen, venstre del av tykktarmen (nærmest endetarmen) og endetarmen. De aller fleste svulstene er lokalisert til nedre venstre del av tykktarmen eller i endetarmen.
Venstre del av tykktarmen og endetarmen
Mørk avføring, endret avføringsmønster, slapphet, vekttap, anfall med magesmerter som følge av passasjeproblemer er mulige symptomer på tarmkreft som kan forekomme uavhengig av om svulsten sitter på høyre eller venstre side av tarmen.
Symptomer som er mer spesifikke for venstre, og siste del av tarmen, er avføringsendringer, blod i avføringen og smerter ved avføring. Disse tegnene gir seg som regel til kjenne tidligere enn symptomene fra en høyresidig svulst
Over halvparten av pasienter med kolorektal kreft har observert blod i avføringen. I noen tilfeller debuterer sykdommen med blodmangel (anemi) der hovedsymptomene er tretthet og blek hud.
Høyre del av tykktarmen
Svulster som sitter i høyre side av tykktarmen kan gi mindre symptomer. Kreftsykdom i denne delen av tarmen gir mer diffuse symptomer som blodmangel, slapphet, nedsatt matlyst, vekttap og eventuelt feber. Det er gjerne blod i avføringen, men blodet trenger ikke være synlig. Dette kalles okkult blødning og kan avsløres med en avføringsprøve som analyseres for blod.
I høyre del av tykktarmen er tarminnholdet mer tyntflytende. Passasjehinderet må derfor være større enn ved venstresidig svulst før tarmen blir blokkert, og man utvikler symptomer på forstoppelse eller stopp i tarmen.
Blokkering av høyre del av tarmen kan gi følgende symptomer:
- Stor mage uten vektøkning
- Uforklarlig vedvarende kvalme og oppkast
- Uforklarlig vekttap
- Vedvarende avføringsendringer i form av endret hyppighet av tarmtømninger og konsistens av avføringen
- Påfallende smalere kaliber på avføringen
- Følelse av ufullstendig tømning etter avføring
Undersøkelsen
Tarmkreft kan være en vanskelig tilstand å oppdage. Ved mistanke om tilstanden vil legen undersøke magen din og kjenne etter oppfylninger og knuter i leveren. Legen vil også kjenne i endetarmen din etter en eventuell svulst eller andre uregelmessigheter.
Legen tar også vanligvis en avføringsprøve for å se om det er tegn til blødning fra tarmen. Blodprøver for blant annet vurdering av blodprosenten (Hb) er viktig. Langvarig blødning kan medføre tap av jern, noe som måles med blodprøven ferritin. Leverprøver tas også for å se om det er tegn til sykdom i leveren.
Rektoskopi er en undersøkelse som først og fremst utføres av en kirurg eller mage-/tarmspesialist. Den foregår ved at et 25 cm langt, stivt rør føres inn i endetarmen slik at legen kan inspisere endetarmen og nederste del av tykktarmen.
I de fleste tilfeller er det nødvendig å gjøre endoskopisk undersøkelse av hele tykktarmen. Koloskopi er en undersøkelse hvor legen benytter en bøyelig, fingertykk slange med kamera som føres inn gjennom endetarmsåpningen. Legen kan slik granske innsiden av hele tykktarmen, og ta vevsprøver av eventuelle mistenkelige forandringer. Bildene fra skopet overføres til en større skjerm slik at du om ønskelig kan følge med selv.
Dersom utredningen avdekker kreft i tykktarm eller endetarm, vil det også bli tatt CT av både lunger, mage og bekken for å kartlegge om det er sykdom utenfor tarmen.
Behandling
Behandlingen av tarmkreft har over tid endret seg fra å være rent kirurgisk til å være en oppgave for et team bestående av kirurger, røntgenleger, patologer og kreftleger. I Norge er det utviklet detaljerte retningslinjer for hvordan kolorektal kreft skal behandles for å sikre best mulig kvalitet og likeverdig tilbud.
Det er flere måter å behandle kolorektal kreft på, avhengig av hvor langt kreften er kommet og hvor svulsten er lokalisert. Hovedbehandlingen er kirurgi. Det er utarbeidet detaljerte standardiserte rutiner for valg av kirurgisk metode. Avhengig av svulstens egenskaper og vekst, om det er spredning eller ei, gis kjemoterapi etter operasjon, eventuelt strålbehandling før eller etter operasjon.
Rundt to av ti pasienter har spredning (fjernmetastaser) på diagnosetidspunktet. I slike tilfeller vil det gjøres en grundig vurdering av om tilstanden kan opereres. Ofte er svaret på dette ja, men først etter forbehandling med kjemoterapi og/eller strålebehandling.
I svært langtkomne tilfeller må en konsentrere seg om å lindre plagene og eventuelt bremse videre vekst og spredning med kjemoterapi, immunterapi eller stråleterapi, såkalt palliativ behandling.
Nye legemidler og nye kombinasjoner av legemidler har gitt bedre resultater med økt overlevelse. Det pågår et intenst forskningsarbeid på dette feltet.
Prognose
Om kreft i tykktarmen oppdages på et tidlig tidspunkt, før svulsten har blitt stor eller spredt seg, er muligheten for helbredelse god. Femårsoverlevelsen for både tykk- og endetarmskreft i tidlig stadium er 98 prosent. Hos de som har fått påvist fjernspredning, vil i gjennomsnitt to av ti leve i minst fem år. De fleste tilfeller av spredning eller tilbakefall kommer innen tre år.
Selv etter en vellykket operasjon, kan det oppstå plager som i stor grad påvirker livskvaliteten. Dette gjelder spesielt etter operasjoner helt ned mot endetarmsåpningen, siden både selve endetarmen og lukkemuskulatur påvirkes. Slike seneffekter kan påvirke evnen til å holde igjen avføring, men kan også gi forstoppelse og andre plager. Tilstanden kalles low anterior resection syndrome, LARS. Det finnes ikke en standardbehandling, men tilstanden kan følges opp av helsepersonell.
Oppfølging
Etter kreftbehandling opplever mange å få vedvarende plager som utmattelse, depresjon, plager med tarm- og blærefunksjon, problemer med seksualitet. Det er viktig å søke råd og hjelp hos helsepersonell for hvordan best mulig bli bedre av eller leve med plagene. Kreftkoordinator i kommunen, fastlege, kreftforeningen er blant ressursene som kan hjelpe.
Det finnes en rekke forskjellige kontrollrutiner, og det er ikke dokumentert hvilket opplegg som er det beste. I Norge anbefales hos de som har hatt dyptvoksende svulster og/eller spredning til lymfeknuter, fem års oppfølging etter en bestemt plan.
Kontrollene startes vanligvis på sykehuset og etterhvert hos fastlegen.
Les mer om oppfølging etter kolorektalkreft
Dette dokumentet er basert på det profesjonelle dokumentet Tykk- og endetarmskreft . Referanselisten for dette dokumentet vises nedenfor
- Helsedirektoratet. Kreft i tykktarm og endetarm - handlingsprogram. Sist faglig oppdatert januar 2026. Siden besøkt 07.04.2026 www.helsedirektoratet.no
- TNM: classification of malignant tumors. (2016). (8 utg.). Oxford: Wiley-Blackwell. www.uicc.org
- Nøkkeltall for kreft. Tykk- og endtarmskreft. Sist endret 23.06.2025. Siden besøkt 07.04.2026 www.fhi.no
- Sinicrope FA. Increasing Incidence of Early-Onset Colorectal Cancer. N Engl J Med. 2022;386(16):1547-1558. PubMed
- GBD 2017 Colorectal Cancer Collaborators. The global, regional, and national burden of colorectal cancer and its attributable risk factors in 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet Gastroenterol Hepatol. 2019 Dec;4(12):913-933. doi: 10.1016/S2468-1253(19)30345-0. Epub 2019 Oct 21. Erratum in: Lancet Gastroenterol Hepatol. 2020 Mar;5(3):e2. PMID: 31648977 PubMed
- Ubago-Guisado E, Rodríguez-Barranco M, Ching-López A et al. Evidence Update on the Relationship between Diet and the Most Common Cancers from the European Prospective Investigation into Cancer and Nutrition (EPIC) Study: A Systematic Review. Nutrients. 2021 Oct 13;13(10):3582. PMID: 34684583 PubMed
- Wang L, Du M, Wang K, et al. Association of ultra-processed food consumption with colorectal cancer risk among men and women: results from three prospective US cohort studies. BMJ 2022; 378: e068921. doi:10.1136/bmj-2021-068921 DOI
- Zepeda-Rivera M, Minot SS, Bouzek H, et al. A distinct Fusobacterium nucleatum clade dominates the colorectal cancer niche. Nature 2024; 628: 424-432. pmid:38509359 PubMed
- Dalla Libera LS, de Siqueira T, Santos IL et al. Detection of Human papillomavirus and the role of p16INK4a in colorectal carcinomas. PLoS One. 2020 Jun 25;15(6):e0235065. PMID: 32584870 PubMed
- Li X, Jansen L, Chang-Claude J, et al. Risk of Colorectal Cancer Associated With Lifetime Excess Weight. JAMA Oncol 2022. pmid:35297997 PubMed
- Hovde Ø, Høivik ML, Henriksen M, et al. Malignancies in Patients with Inflammatory Bowel Disease: Results from 20 Years of Follow-up in the IBSEN Study. Journal of Crohn's and Colitis, 2017; 11 (5): 571–577. academic.oup.com
- Brenne SS, Madsen PH, Pedersen IS, et al. Colorectal cancer detected by liquid biopsy 2 years prior to clinical diagnosis in the HUNT study published online ahead of print, 2023 Jul 12. Br J Cancer. 2023;10.1038/s41416-023-02337-4. PMID: 37438612 PubMed
- Juul FE, Cross AJ, Schoen RE, et al. 15-Year Benefits of Sigmoidoscopy Screening on Colorectal Cancer Incidence and Mortality : A Pooled Analysis of Randomized Trials. Ann Intern Med 2022. pmid:36215714 PubMed
- Bretthauer M, Loberg M, Wieszczy P, et al. Effect of Colonoscopy Screening on Risks of Colorectal Cancer and Related Death. N Engl J Med. 2022. PMID: 36214590 PubMed
- Randel KR, Schult AL, Botteri E, et al. Colorectal cancer screening with repeated fecal immunochemical test versus sigmoidoscopy: baseline results from a randomized trial published online ahead of print, 2020 Nov 20. Gastroenterology. 2020;S0016-5085(20)35440-8. PMID: 33227280. PubMed
- Cardoso R, Guo F, Heisser T, et al. Colorectal cancer incidence, mortality, and stage distribution in European countries in the colorectal cancer screening era: an international population-based study. Lancet Oncol. 2021 Jul;22(7):1002-1013. Epub 2021 May 25. PMID: 34048685 PubMed
- Bretthauer M, Kaminski MF, Løberg M, et al. Population-based colonoscopy screening for colorectal cancer. JAMA Intern Med 2016; 176: 894-902. doi:10.1001/jamainternmed.2016.0960 DOI
- Edna TH, Karlsen V, Jullumstrø E, Lydersen S. Prevalence of anaemia at diagnosis of colorectal cancer: assessment of associated risk factors. Hepatogastroenterology 2012; 59: 713-6. PubMed
- Gjør kloke valg. Norsk forening for medisinsk biokjemi. Unngå å bestille tumormarkører, særlig CEA, CA-125, HE4, AFP og CA19-9 når det ikke foreligger kjent kreftsykdom, spesifikk mistanke om en bestemt krefttype eller en sterk, underliggende predisposisjon. 04.07.2018 www.legeforeningen.no
- Gjør kloke valg. Norsk forening for medisinsk biokjemi. Unngå test for okkult blod i avføringen ved andre indikasjoner enn mistanke om kolorektal kreft. Kvantitative immunologiske tester for okkult blod (iFOBT) bør erstatte kjemiske tester. Publisert 9. januar 2023. www.legeforeningen.no
- Lee JK, Liles EG, Bent S, et al. Accuracy of fecal immunochemical tests for colorectal cancer: Systematic review and meta-analysis. Ann Intern Med 2014; 160: 171-81. doi:10.7326/M13-1484 DOI
- Randel KR, Botteri E, Romstad KMK, et al. Effects of Oral Anticoagulants and Aspirin on Performance of Fecal Immunochemical Tests in Colorectal Cancer Screening. Gastroenterology 2019. doi:10.1053/j.gastro.2019.01.040 DOI
- Gao Y, Wang J, Lv H, et al. Diagnostic value of magnetic resonance and computed tomography colonography for the diagnosis of colorectal cancer: A systematic review and meta-analysis. Medicine (Baltimore). 2019;98(39):e17187. PMID: 31574825. PubMed
- Konishi T, Shimada Y, Hsu M, et al. Association of Preoperative and Postoperative Serum Carcinoembryonic Antigen and Colon Cancer Outcome. JAMA Oncology 2018; 4: 309-315. pmid: 29270608 PubMed
- Aune D, Chan DSM, Lau R, et al. Dietary fibre, whole grains, and risk of colorectal cancer: systematic review and dose-respons meta-analysis of prospective studies. BMJ 2011; 343: d6617. BMJ (DOI)
- Yang B, Jacobs EJ, Gapstur SM, et al. Active Smoking and Mortality Among Colorectal Cancer Survivors: The Cancer Prevention Study II Nutrition Cohort. J Clin Oncol 2015; 33: 885-93. doi:10.1200/JCO.2014.58.3831 DOI
- Van Blarigan EL, Fuchs CS, Niedzwiecki D et al. Association of Survival With Adherence to the American Cancer Society Nutrition and Physical Activity Guidelines for Cancer Survivors After Colon Cancer Diagnosis The CALGB 89803/Alliance Trial. JAMA Oncol 2018; 4: 783-790. pmid:29710284 PubMed
- Yao Y, Suo T, Andersson R, et al. Dietary fibre for the prevention of recurrent colorectal adenomas and carcinomas. Cochrane Database of Systematic Reviews 2017, Issue 1. Art. No.: CD003430. DOI: 10.1002/14651858.CD003430.pub2. DOI
- Rothwell PM, Wilson M, Elwin C-E, et al. Long-term effect of aspirin on colorectal cancer incidence and mortality: 20-year follow-up of five randomised trials. Lancet 2010; 376: 1741-50. PubMed
- Friis S, Riis AH, Erichsen R, et al. Low-dose aspirin and nonsteroidal anti-inflammatory drug use and colorectal cancer risk: A population-based, case-control study. Ann Intern Med 2015. doi:10.7326/M15-0039 DOI
- Rothwell PM, Price JF, Fowkes FGR, et al. Short-term eff ects of daily aspirin on cancer incidence, mortality, and non-vascular death: analysis of the time course of risks and benefi ts in 51 randomised controlled trials. Lancet 2012; : DOI:10.1016/S0140-. DOI
- Burn J, Sheth H, Elliott F, et al. Cancer prevention with aspirin in hereditary colorectal cancer (Lynch syndrome), 10-year follow-up and registry-based 20-year data in the CAPP2 study: a double-blind, randomised, placebo-controlled trial. Lancet North Am Ed 2020;395:1855–63. PMID: 32534647 PubMed
- Nafisi S, Støer NC, Veierød MB, et al. Low-Dose Aspirin and Prevention of Colorectal Cancer: Evidence From a Nationwide Registry-Based Cohort in Norway. Am J Gastroenterol 2024; 119: 1402-1411. pmid:38300127 PubMed
- Kreftregisteret. Cancer in Norway 2024. Oslo: Kreftregisteret, 2024, www.kreftregisteret.no. www.fhi.no
- Jeffery M, Hickey BE, Hider PN. Follow‐up strategies for patients treated for non‐metastatic colorectal cancer. Cochrane Database of Systematic Reviews 2019, Issue 9. Art. No.: CD002200. DOI: 10.1002/14651858.CD002200.pub4. DOI
- Keys MT, Serra-Burriel M, Martínez-Lizaga N et al. Population-based organized screening by faecal immunochemical testing and colorectal cancer mortality: a natural experiment. Int J Epidemiol. 2021 Mar 3;50(1):143-155. PMID: 33211822. PubMed